Craspedacusta sowerbyi : minuscule mais si visible !
Par Alain Dutartre
Il n’est apparemment pas nécessaire d’être de grande taille ni de se manifester de manière permanente dans les milieux aquatiques pour être reconnue comme une espèce exotique envahissante. Il suffit de mesurer un peu plus de 15 mm de diamètre, de flotter dans les eaux comme une ombrelle blanche presque transparente, de s’ouvrir et se fermer sur un rythme quasi cardiaque, pour attirer les regards, juste un peu de mystère et de surprise qui provoquent une multiplicité des écrits et de diffusion d’informations.
C’est ainsi que la méduse d’eau douce Craspedacusta sowerbyi a fait récemment fait l’objet de deux publications présentant de nouvelles observations, en 2013 en Aquitaine et en 2014 en Bretagne. Ce sont deux références de plus sur cette espèce qui en compte déjà des milliers : dans son article de 2010, Marie-José Turquin précise qu’en octobre 2009 le moteur de recherche Google listait déjà 55 000 références pour C. sowerbii et 35 300 pour C. sowerbyi (parce qu’en plus cette espèce bénéficie de deux orthographes). On pourra d’ailleurs se référer à son article qui contient de très nombreuses informations sur la biologie, l’écologie et la répartition dans le monde de cette méduse.
Depuis sa découverte à Londres en juin 1880, cette espèce a été observée dans tous les pays du monde et dans de très nombreux types de milieux aquatiques d’eau douce, pas seulement dans de “petites collections d’eau” mais aussi dans des lacs, des grands cours d’eau, etc.
Sa dispersion est très largement facilitée par son mode de reproduction présentant une alternance de polypes sessiles asexués et les méduses mobiles sexuées. Les polypes sous forme enkystée peuvent subsister plusieurs années. Ils peuvent être transportés fixés sur des plantes aquatiques, elles-mêmes transportées d’un continent à un autre comme ce fut le cas de la jacinthe d’eau (Eichhornia crassipes) ou du lotus géant (Victoria regia), deux espèces fréquemment citées comme vecteurs d’introduction. D’autres organismes comme les poissons ou les oiseaux peuvent aussi servir de vecteurs, et Turquin (2010) signale également les engins de travaux publics, les extractions et transports de granulats comme un moyen de dispersion plus localisé.
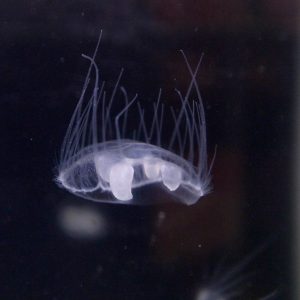
Les polypes fixés dans le milieu peuvent produire trois sortes de bourgeons, dont des bourgeons médusaires qui donnent de petites méduses se séparant du polype par des “contractions vigoureuses de l’ombrelle” (Turquin, 2010). Les méduses sont sexuées mais les deux sexes coexistent très rarement aussi leur reproduction est-elle de fait asexuée.
L’apparition des méduses est sporadique et son facteur de déclenchement semble être la température des eaux. Des travaux de laboratoire ont montré que les bourgeons médusaires ne se forment qu’entre 26 et 33 °C et les observations se produisent d’ailleurs la plupart du temps en été dans des eaux chaudes. Les méduses peuvent toutefois continuer à se déplacer en pleine eau “tant que la température dépasse 14,5 °C ; en dessous elles tombent au fond et se rétractent en boule. Si la température remonte, elles peuvent reprendre une nage active” (expériences de THOMAS, 1951, citées par Turquin, 2010).
Cette nage est en fait ce qui attire le regard sur cette minuscule espèce : il suffit pour s’en convaincre d’aller voir, parmi d’autres, les vidéos suivantes :
- https://www.youtube.com/watch?v=UFPkkW-EmAs
- http://www.dailymotion.com/video/xu90q0_craspedacusta-sowerbyi_animals
La plupart des auteurs indiquent que l’origine de cette espèce est le Yang Tsé Kiang. La multiplicité des observations la concernant depuis 130 ans sur tous les continents (sauf l’Antarctique) en fait évidemment une espèce exotique envahissante et c’est d’ailleurs pour cette raison qu’elle figure par exemple dans les fiches présentes sur le site NOBANIS (http://www.nobanis.org/). Toutefois, comme le rappelle Turquin (2010), “son impact écologique est négligeable“.
Même si dans certains cas les méduses peuvent être très nombreuses, les densités citées par différents auteurs sont extrêmement variables, de moins d’un individu à plus de 1000 par m². Les recherches menées sur la consommation de zooplancton par les méduses (citées dans l’article de Turquin, 2010) ont comporté des expérimentations en microcosmes et des examens de contenus stomacaux des méduses. Les proies consommées mesurent de 0,2 à 2 mm.
Ce sont des micro-crustacés herbivores, des copépodes, des rotifères, etc. Ces recherches donnent également des résultats très variables avec des estimations de consommation journalière de différentes proies mais, même si quelques auteurs estiment que la présence de C. sowerbii a “la possibilité de modifier de manière significative les communautés zooplanctoniques et, par conséquent, les réseaux trophiques aquatiques”, la plupart d’entre eux concluent en jugeant faibles les impacts sur les peuplements de zooplancton et les chaînes alimentaires.
Les apparitions sporadiques et généralement de courte durée des méduses contribuent sans doute largement à rendre cette espèce invasive sans impact écologique significatif sur les milieux aquatiques mais l’étrangeté de ses ombrelles mobiles continuera à alimenter les parutions d’articles, y compris ceux de la presse régionale estivale, toujours à la recherche d’éléments extraordinaires.
- En savoir plus : Consultez les articles suivants :
Nouvelles découvertes en Aquitaine de la méduse d’eau douce Craspedacusta sowerbii
Quelques mentions de la méduse d’eau douce Craspedacusta sewerbii en Loire-Atlantique
Progrès dans la connaissance de la métagénèse chez Craspedacusta sewerbii


