Établissement, propagation et premiers impacts d’un agent de biocontrôle introduit contre une plante exotique envahissante au Portugal
La publication de Lopez-Núnez et al. (2021) présente les résultats de cinq années d’un programme d’introduction au Portugal d’une petite guêpe d’origine australienne, Trichilogaster acaciaelongifoliae, spécifique d’un arbuste ou petit arbre de même origine, Acacia longifolia, introduit depuis le XIXème siècle dans différents pays à des fins ornementales ou pour stabiliser les dunes. En pondant ses œufs dans les bourgeons floraux et végétatifs de la plante, la guêpe provoque la formation de galles qui peuvent réduire très fortement la production de graines et la croissance végétative de son hôte.
Cette guêpe a déjà été utilisée au début des années 80 comme agent de contrôle biologique d’A. longifolia en Afrique du Sud avec de très bons résultats. C’est pourquoi l’équipe de recherches ayant réalisé ces travaux réunit deux laboratoires portugais de Coimbra (Centre d’écologie fonctionnelle de l’Université et École supérieure d’agriculture) et deux laboratoires sud-africains (Université de Cape Town et Conseil de recherche agricole de Stellenbosch).
L’espèce à contrôler
Originaire du sud-est de l’Australie, Acacia longifolia (Andr.) Willd. (Acacia à feuilles longues, Mimosa à longues feuilles) a été introduit depuis le XIXème siècle dans différents pays à des fins ornementales et pour stabiliser les dunes (Kull et al., 2011). Cet arbuste ou petit arbre pouvant atteindre 8 m de hauteur présente des feuilles persistantes, réduites à des phyllodes (pétiole aplati assurant une fonction assimilatrice similaire à celle des feuilles). La floraison se produit de décembre à avril. Ses fleurs sont jaune vif, réunies en épis axillaires. Ses fruits sont des gousses cylindriques, déformées à maturité.
L’espèce présente d’importantes capacités de colonisation et de compétition, une croissance rapide, une abondante production de graines (jusqu’à 11 500 graines/m2/an) (Gibson et al., 2011), qui peuvent rester viables dans le sol pendant longtemps (Marchante et al., 2010). Elles sont dispersées par des animaux, principalement des oiseaux et des fourmis. L’espèce présente un comportement pyrophytique et la germination est stimulée par le feu.
Comme d’autres espèces d’acacia, A. longifolia est un arbuste qui fixe l’azote et produit de grandes quantités de litières à décomposition lente. Ces litières peuvent s’accumuler en couches épaisses sous la canopée des peuplements denses et presque monospécifiques colonisant les dunes que l’espèce peut développer dans des conditions favorables. Comme ces dunes sont naturellement dépourvues de litières, ces peuplements réduisent la biodiversité et perturbent les cycles des nutriments et de l’eau ainsi que les régimes d’incendie (voir par exemple Marchante et al., 2015). Cependant, dans des zones de sous-bois, son développement peut être fortement réduit.

L’espèce est actuellement considérée comme envahissante en Argentine, au Brésil, en Nouvelle-Zélande, en Espagne, en Afrique du Sud et au Portugal (CABI, 2019).
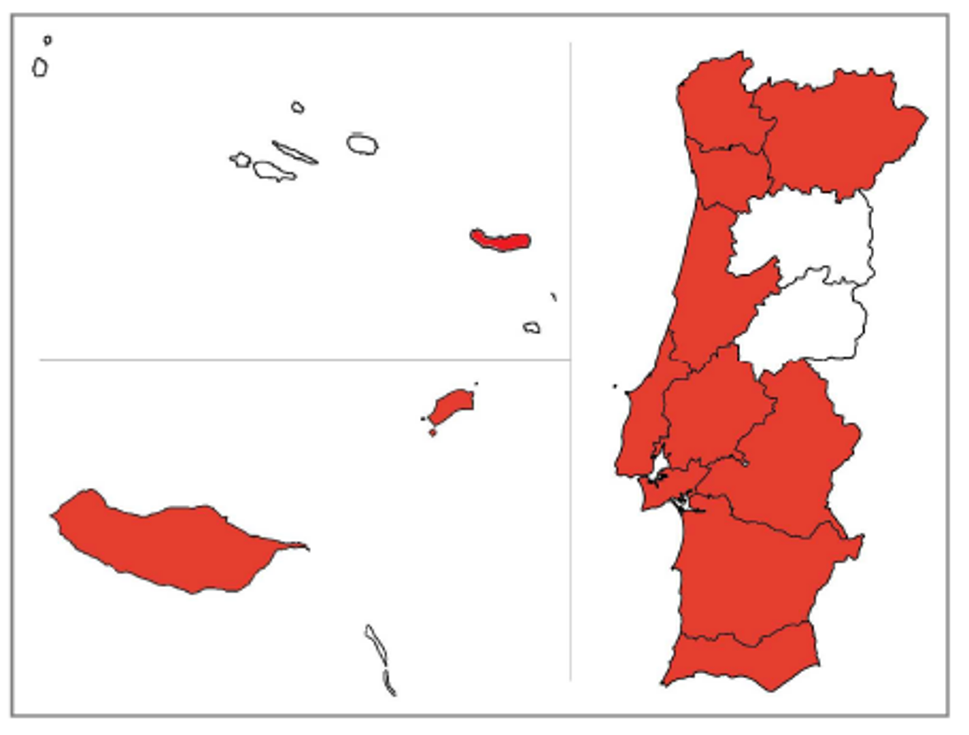
Au Portugal, selon Marchante et al. (2011a), A. longifolia est même l’espèce exotique envahissante la plus répandue dans les dunes littorales du pays. Elle y a été introduite au début du 20ième siècle pour y freiner l’érosion. A partir des plantations réalisées à cette fin, l’espèce s’est largement dispersée à la suite d’incendies, avec des conséquences écologiques diverses qui se sont intensifiées au fil des années.
Selon Marchante et al. (2009), elle est présente dans toutes les régions littorales portugaises continentales (Trás-os-Montes, Minho, Douro Litoral, Beira Litoral, Estremadura, Ribatejo, Alto Alentejo, Baixo Alentejo, Algarve), dans l’île de Santa Maria dans l’archipel des Açores et dans l’archipel de Madère (îles de Madère et de Porto Santo).
Elle a un statut d’espèce exotique envahissante avec un niveau de risque de 30 selon le protocole adapté de l’Australian Weed Risk Assessment (Pheloung et al. 1999), pour lequel des valeurs supérieures à 6 correspondent à des risques d’invasion significatifs.
L’agent de contrôle
Hyménoptère de la famille des Pteromalidae, Trichilogaster acaciaelongifoliae est une guêpe originaire du sud-est de l’Australie spécifique de A. longifolia s. l. (Noble, 1940).

D’une taille de 2 à 3 mm, elle pond ses œufs dans les bourgeons floraux et végétatifs de la plante. Les larves provoquent ensuite la formation d’une galle qui se développe en une sphère autour d’elle (Henriksen et al, 2017) inhibant le développement de la fleur et des phyllodes.

Ces galles peuvent comporter une ou plusieurs chambres abritant chacune une larve. La plupart des chambres contiennent des femelles, mais parfois les mâles se développent dans des chambres plus petites à la périphérie de la galle (Marchante et al., 2011b).
Dans les cas d’infestation massive, la production de graines de l’arbuste peut ainsi être réduite de 99 % (Dennill, 1985) et sa croissance inhibée. Des mortalités occasionnelles peuvent se produire avec des biomasses de galles pouvant représenter jusqu’à 21 % de la biomasse sèche des parties aériennes des arbres colonisés provoquant la rupture et la mortalité de grosses branches et de tiges (Dennill, 1988).
Cette espèce est univoltine (une génération par an). Dans l’hémisphère sud, les guêpes émergent des galles à la fin de l’été, avec un pic d’émergence en novembre. Les guêpes adultes vivent généralement de 1 à 3 jours (rarement jusqu’à 7). Les femelles pondent en moyenne 300 à 400 œufs, de préférence dans les petits bourgeons floraux (< 2 mm), et moins fréquemment dans les bourgeons végétatifs (Noble, 1940). Les femelles de cette espèce sont parthénogénétiques et peuvent donc se reproduire sans mâle.
N.B. : Des compléments d’information sur la biologie et l’écologie de l’espèce sont par exemple à consulter dans l’article de Henriksen et al. (2017) (“Gall wasp biocontrol of invasive Acacia longifolia: implications of strong bottom-up effects“).
Après différents travaux en Australie sur l’écologie de l’espèce et sa spécificité sur quelques espèces d’acacia indigènes, dont A. longifolia, elle a été introduite intentionnellement pour la première fois en Afrique du Sud au début des années 80 (Dennill, 1988). Selon EFSA PLH Panel (2015), elle était alors présente dans toute l’aire de répartition d’A. longifolia dans ce pays, la plupart des plantes présentant des galles et des réductions de la formation des graines pouvant atteindre 95 %. La réduction de croissance végétative pouvait atteindre 30 % (Dennill, 1985, 1988). Après ce succès obtenu en Afrique du Sud, l’utilisation de T. acaciaelongifoliae a été envisagée au Portugal. L’espèce pouvant infester d’autres espèces que A. longifolia (dont A. floribunda cultivée comme plante ornementale à petite échelle en France, en Grèce et en Italie et non considérée comme envahissante dans l’UE) des tests de spécificité d’hôte ont été réalisés.
Au cours du processus d’obtention de l’autorisation de lâcher, une évaluation de risque a été réalisée par le Groupe scientifique sur la santé des plantes de l’EFSA (Autorité européenne de sécurité des aliments) . Dans les conclusions du document produit par ce groupe de travail figuraient, entre autres, les commentaires suivants :
- les conditions climatiques dans l’UE étaient largement adaptées à l’établissement de T. acaciaelongifoliae,
- l’espèce pourrait être intentionnellement déplacée pour contrôler des populations d’A. longifolia autres que celles présentes au Portugal,
- il était moyennement probable qu’elle puisse s’établir et se disséminer dans l’UE par des moyens naturels,
- les impacts d’A. longifolia sur la biodiversité et les écosystèmes indigènes colonisés pouvaient être réduits par T. acaciaelongifoliae.
Un autre commentaire rappelait que la probabilité d’établissement d’une population fondatrice dépendait de la capacité à faire coïncider le cycle biologique de la guêpe (originaire de l’hémisphère sud) avec la phénologie de l’hôte dans l’hémisphère nord.
Acclimatation
L’établissement d’un agent de biocontrôle est évidemment influencé par de nombreux facteurs tels que le nombre d’agents libérés et le moment de ces libérations, les conditions météorologiques, et la synchronisation phénologique entre la plante-hôte et l’agent de biocontrôle. Dans leur analyse mondiale des introductions, des taux d’établissement et des estimations de réussite de contrôle biologique Schwarzländer et al. (2018) signalaient un taux d’établissement généralement élevé (70,9 %) pour 468 agents introduits intentionnellement et utilisés contre des espèces végétales envahissantes. Cependant les implications de translocations entre les hémisphères du globe n’étaient pas encore analysées.
Les objectifs des présents travaux étaient donc : 1) de surveiller l’établissement et la propagation précoce de T. acaciaelongifoliae au Portugal ; 2) d’analyser les implications du changement d’hémisphère dans l’établissement de la guêpe en comparant l’établissement des populations importées et portugaises ; et 3) d’évaluer les impacts initiaux de T. acaciaelongifoliae sur la production végétative et reproductive de la plante cible, A. longifolia.
Avec l’autorisation de l’Institut pour la conservation de la nature et de la biodiversité (ICNB), des galles matures de T. acaciaelongifoliae ont été expédiées en 2015 depuis l’Afrique du Sud pour obtenir des guêpes femelles adultes à libérer dans différents sites de la côte portugaise (Marchante et al., 2011 ; Shaw et al., 2016).
Dans sa thèse consacrée à l’invasion des dunes du Portugal par A. longifolia et aux perspectives de son contrôle, Helia Marchante (2011) a évalué les possibilités d’acclimatation au Portugal de T. acaciaelongifoliae. Dans ses travaux réalisés en Afrique du Sud et au Portugal, elle a également testé la spécificité de la guêpe sur différentes espèces végétales et les conditions de synchronisation phénologique de cette translocation d’un hémisphère à l’autre.

C’était en effet une importante préoccupation concernant l’établissement de l’espèce introduite. Pendant les campagnes au Portugal de lâchers de guêpes importées (novembre – début janvier), le nombre de plants d’A. longifolia portant des bourgeons de taille adéquate pour accueillir les pontes était faible car la majorité des bourgeons se développent plus précocement dans l’année, entre mai et juin (Morais et Freitas, 2015). Il était donc essentiel de surveiller l’établissement et la propagation de T. acaciaelongifoliae et d’évaluer si une synchronisation de son cycle de vie avec la phénologie d’A. longifolia était possible dans l’hémisphère nord.
Les sites

La côte atlantique portugaise est caractérisée par des dunes où la végétation indigène a été largement remplacée par A. longifolia et d’autres espèces de plantes exotiques envahissantes, comme Carpobrotus edulis. Le climat est principalement méditerranéen avec des étés chauds. La région la plus au sud (et aux températures estivales plus élevées) présente un climat très similaire à l’aire d’invasion d’A. longifolia en Afrique du Sud.
Afin d’augmenter la probabilité d’établissement et de promouvoir une large distribution de T. acaciaelongifoliae, des lâchers ont été effectués dans 61 sites, principalement le long de la côte. Entre novembre et début janvier 2015, 2016 et 2017, 2 073 galles matures de T. acaciaelongifoliae ont été importées depuis l’Agriculture Research Council-Plant Health and Protection de Stellenbosch (Afrique du Sud). Elles ont été conservées en quarantaine puis, après éclosion, des femelles de T. acaciaelongifoliae ont été relâchées dans les sites présélectionnés dans les 36 heures suivant leur émergence. En juin 2018, 1 091 galles matures ont été collectées dans une population nouvellement établie à São Pedro de Moel. Elles ont été maintenues dans des conditions de laboratoire similaires à celles des galles importées et des femelles saines nouvellement émergées de ces galles formées au Portugal ont été relâchées. En 2019, 73 galles supplémentaires provenant de populations portugaises établies ont été relâchées dans deux sites supplémentaires. Au total, entre 2015 et 2019, 3 567 guêpes femelles ont ainsi été relâchées dans les 61 sites (Fig.3).
Protocole de suivi de l’établissement de T. acaciaelongifoliae
Quatre des 61 sites de lâcher (São Jacinto dunes, Quiaios, Coimbra et São Pedro de Moel) ont été sélectionnés pour un suivi régulier. Sur chacun de ces sites, 3 à 6 guêpes femelles par arbre ont été lâchées sur au moins 25 plants d’A. longifolia sains. Les arbres choisis étaient espacés d’un minimum de 20 m. Sur chacun d’entre eux, trois branches présentant des bourgeons sains immatures (< 2 mm) ont été sélectionnées, marquées, et une guêpe a été délicatement placée (« a single wasp was gently placed on one phyllode ») sur un phyllode de chaque branche, à proximité d’un bourgeon. En tant que points de dispersion initiaux, la localisation de ces branches a été réalisée avec un GPS de précision submétrique.
Méthodes de suivis
Établissement et suivi de T. acaciaelongifoliae
Ces quatre sites ont été visités mensuellement et les arbres test ont été inspectés entre mars et juillet, période de développement floral et végétatif. Des visites supplémentaires ont eu lieu en automne et en hiver pour évaluer la synchronisation du cycle de vie de T. acaciaelongifoliae avec son hôte dans l’hémisphère nord en vérifiant l’apparition des galles. Après 2017, les populations de T. acaciaelongifoliae semblaient s’être synchronisées avec A. longifolia, et la surveillance a été limitée entre la fin du printemps et le début de l’été.
Lors de chaque visite, les branches marquées ont été inspectées pour noter : i) Le nombre de galles par branche ; ii) Le nombre de chambres par galle (observation externe) ; et iii) La coordonnée GPS de chaque galle ou groupe de galles physiquement attachées.
En 2016 et 2017, des galles ont été activement recherchées à proximité des arbres tests pour un comptage total. En 2018, la croissance exponentielle du nombre de galles observées sur les quatre sites a rendu pratiquement impossible le maintien de ce comptage absolu. Il a donc été procédé à un échantillonnage sur une partie des branches et à des estimations des nombres totaux de galles.
En 2019, les fortes accumulations de galles et la large dispersion des guêpes dans les sites ont rendu impossible la détection de toutes les branches portant des galles. La densité de galles a alors été estimée à l’aide de deux méthodes d’estimation (non détaillées ici) appliquant toutefois des protocoles rigoureux : dans trois des sites il s’agissait de comptages par déplacement sur des transects, dans le quatrième d’observations circulaires à l’aide de jumelles.
Par ailleurs, entre 2015 et 2017, la distance annuelle maximale de dispersion de la guêpe depuis les arbres test a été estimée sur les quatre sites.
Impact de T. acaciaelongifoliae sur A. longifolia

L’impact de T. acaciaelongifoliae sur la croissance végétative et reproductive d’A. longifolia a été évalué sur trois des sites de surveillance (São Jacinto, São Pedro de Moel et Quiaios). Entre 2018 et 2020, 59 arbres porteurs de galles et 62 arbres non-porteurs ont été évalués sur ces sites. Sur chacun des arbres porteurs, des branches elles-mêmes porteuses ou non de galles ont été sélectionnées ; des branches ont également été sélectionnées au hasard sur les arbres non-porteurs. Toutes ont été marquées, géolocalisées et divers paramètres ont été notés (longueur de la branche, nombre de branches secondaires, nombre de phyllodes, de gousses et de graines). Au total, 390 branches marquées en 2018 ont été aussi mesurées en 2019, et 510 branches supplémentaires marquées en 2019 sur de nouveaux arbres ont aussi fait l’objet de mesures en 2020.
Des analyses statistiques non détaillées ici, utilisant différents modèles linéaires mixtes généralisés (GLMM), ont été utilisées pour interpréter toutes les données recueillies.
Résultats
Établissement et propagation de T. acaciaelongifoliae
En 2020, cinq ans après le début des lâchers de T. acaciaelongifoliae au Portugal, l’établissement de l’espèce avait été confirmé sur 36 des 61 sites de lâchers.
 |
 |
Fig. 4 : (a) Expansion spatiale de la population de T. acaciaelongifoliae de 2016 à 2018 dans les quatre sites de suivi régulier. Notez les différentes échelles dans chaque photo aérienne. (b) Nombre de galles détectées de 2016 à 2018, au printemps et au début de l’été (mars-juillet), dans les quatre sites. (c) Distances atteintes par T. acaciaelongifoliae chaque année, depuis les arbres de lâcher jusqu’à la galle la plus éloignée détectée. Dans (b) et (c), les barres d’erreur représentent l’erreur standard, n = 4. Les lettres indiquent les résultats d’un test statistique. Extrait de Lopez-Núnez et al. (2021).
Le succès d’établissement a rapidement évolué, passant de 0 % en 2018 (guêpes sud-africaines lâchées sur 16 sites en 2017) à 84,8 % en 2019 et 100 % en 2020 (guêpes portugaises lâchées sur respectivement 33 sites en 2018 et 2 sites en 2019. Le nombre comptabilisé de galles a très rapidement augmenté soit 24 793 galles en 2018, dernière année où il était possible d’estimer le nombre total de galles observées.
Entre 2016 et 2018, le nombre de galles observées a significativement augmenté chaque année, notamment de 2017 à 2018 (fig. 4 ; moyennes et erreurs standards respectivement de 331 ± 136 à 6 167 ± 3 593). En 2019, le nombre de galles a continué d’augmenter, avec un maximum de 298 galles/m² à Coimbra. Cependant, comme la méthode de suivi a dû être modifiée pour s’adapter à l’augmentation des nombres de galles, il n’a pas été possible de comparer statistiquement ces résultats.
La distance de dispersion a également augmenté de manière significative de 2015 à 2018. La première année de suivi (2016), les galles de T. acaciaelongifoliae n’ont été trouvées qu’à proximité immédiate des arbres de lâcher, soit en moyenne environ 3 m, puis un et deux ans après le lâcher (2017 et 2018), ces distances moyennes étaient respectivement de 13 et 223 m. En 2019, certaines galles ont même été observées à 7 km de l’arbre de lâcher le plus proche (données non publiées). Notons enfin que le nombre de chambres par galle pouvait varier d’une à douze, soit près de 2 en moyenne, ce qui peut permettre d’estimer la population de guêpes présentes chaque année.
Impacts de T. acaciaelongifoliae sur A. longifolia
Au cours de ces quelques années le nombre total d’arbres porteurs de galles est resté relativement faible. Cependant, certains impacts positifs de T. acaciaelongifoliae ont déjà pu être observés sur la croissance reproductive et végétative d’A. longifolia.
Par exemple, la production de gousses et de graines a été significativement réduite dans les arbres porteurs par rapport aux arbres non-porteurs, respectivement de 84,1 % et 95,2 %. Le nombre de branches secondaires a également été réduit de 33,3 % dans les arbres porteurs.
 |
 |
Fig.5 : (a) Impacts de T. acaciaelongifoliae sur le nombre de graines, de gousses, de branches secondaires, de phyllodes, et la longueur totale des branches d’A. longifolia (pourcentages moyens entre les périodes 2018-19 et 2019-20, sur les trois sites suivis). (b) Impact de T. acaciaelongifoliae sur la production reproductive et végétative d’A. longifolia (pourcentages de changement observé sur les arbres porteurs de galles par rapport aux valeurs de référence des arbres non porteurs). Extrait de Lopez-Núnez et al. (2021).
Les auteurs indiquent également avoir observé sur les arbres porteurs de galles des tendances non statistiquement significatives, en particulier une production plus faible de phyllodes de 28,5 %.
Discussion et conclusion
Suite aux premières libérations de 2015, T. acaciaelongifoliae s’est donc bien établi avec succès sur A. longifolia dans différents sites des zones côtières du Portugal. Dans la discussion très complète de leurs résultats, les auteurs passent en revue les caractéristiques et contraintes de cette expérimentation et les perspectives à attendre de ce succès.
Les premières guêpes issues de galles importées d’Afrique du Sud ont été libérées en hiver à une période peu favorable au développement des bourgeons appropriés pour la ponte (Marchante et al., 2011), expliquant probablement le faible taux de réussite des premiers lâchers. Les années suivantes, les guêpes issues des galles développées au Portugal ont pu éclore en fin du printemps et au début de l’été, période de développement des bourgeons d’A. longifolia (Morais et Freitas, 2015) facilitant ainsi les pontes et donc l’établissement de l’espèce.
Cette évolution a été similaire à celle observé en Afrique du Sud lorsque T. acaciaelongifoliae a été introduit depuis l’Australie (Dennill, 1987). Une comparaison de l’effort de lâcher sur les quatre principaux sites de surveillance au Portugal en 2015 et des premiers lâchers à Stellenbosch, en Afrique du Sud, en 1981, montrait que des nombres assez proches de guêpes avaient été introduites dans les deux cas. Cependant le nombre de guêpes issues des galles de seconde génération au Portugal était plus faible d’environ un facteur de 10 par rapport à celui des guêpes signalées en Afrique du Sud (Dennill, 1987), ce qui, selon les auteurs, confirme que lors de son introduction T. acaciaelongifoliae a dû surmonter au Portugal certaines barrières de compatibilité (dont le changement d’hémisphère influant sur la phénologie de la plante et les conditions climatiques du Portugal), ce qui n’était pas le cas pour l’Afrique du Sud.
Bien que les impacts de T. acaciaelongifoliae sur la plante hôte n’aient été mesurés qu’en 2019 et 2020, les résultats de ces investigations démontrent bien une forte diminution des capacités reproductives des individus d’A. longifolia avec de très faibles productions de gousses et donc de graines. Les impacts sur leur développement végétatif des arbres par la concurrence pour les ressources nutritives occasionnée par le développement des galles sont moins perceptibles.
Les auteurs rappellent que la fréquence croissante d’événements météorologiques et climatiques extrêmes que connait le Portugal, tels que les vagues de chaleur et les sécheresses, peuvent affecter l’établissement et la propagation ultérieure de la guêpe. Les galles sont sensibles à la dessiccation ce qui peut nuire à la viabilité des œufs ou des larves de T. acaciaelongifoliae (Dennill et Gordon, 1990).
Ils listent également les limites de ces premiers travaux sur cette introduction, dont celles inhérentes à une expérimentation de gestion réalisée en milieu naturel, nécessairement moins rigoureuse dans la mise en œuvre concrète qu’un plan expérimental « purement scientifique » (« a purely scientific experimental design »). L’étendue et l’hétérogénéité des zones colonisées par A. longifolia, la forte densité des arbres dans certains peuplements sont autant de limites pratiques aux observations pouvant par exemple induire des sous-estimations des détections des galles. Des adaptations des méthodes de suivi de terrain à plus long terme seraient sans doute nécessaires.
De même, des interférences sur l’établissement et le maintien des populations de T. acaciaelongifoliae peuvent se produire, comme cela a déjà été le cas sur plusieurs sites pour diverses raisons (incendies de forêt, interventions forestières, abattage illégal ou tempêtes extrêmes).
Commentaires
Quoi qu’il en soit, les résultats de ces travaux démontrent le succès initial de cette introduction d’un agent de biocontrôle libéré intentionnellement avec une extension portugaise déjà notable en quelques années. Ces résultats prometteurs pourraient tout à fait participer à l’évolution des représentations portées en Europe sur les possibilités de contrôle biologique des EEE et contribuer au développement de futurs programmes de biocontrôle.
Selon Shaw et al. (2018) cette évolution est déjà en cours depuis quelques années. Dans cette publication les auteurs présentent un bilan appuyé sur quelques exemples démonstratifs d’introductions d’agents de contrôle biologique de plantes exotiques envahissantes en Europe. Parmi ces introductions, toutes bénéfiques, quelques-unes sont accidentelles (la plus connue étant celle du charançon Stenopelmus rufinasus, consommateur efficace d’Azolla filiculoides) mais les plus récentes sont des introductions intentionnelles. Ils en infèrent que l’Union Européenne est en train de passer d’une période de sérendipité (découverte inattendue et fructueuse) à une période de stratégie (“from a period of serendipity to a period of strategy »).
Au final, il nous semble que ces résultats de travaux de recherche appliqués à la gestion d’espèces jugées problématiques illustrent surtout, s’il en était encore besoin, l’incontestable nécessité de la coopération scientifique mondiale, ici entre deux territoires lointains de l’autre hémisphère de la planète et notre continent, pour espérer devenir collectivement de meilleurs administrateurs de ces espèces que nous continuons de transporter consciemment ou non.
Rédaction : Alain Dutartre, expert indépendant
Relectures et contributions : Madeleine Freudenreich et Emmanuelle Sarat, Comité français de l’UICN
Illustration-bandeau : Galles de Trichilogaster acaciaelongifoliae – JonRichfield, CC BY SA 3.0
Pour en savoir plus :
A propos de contrôle biologique :
- 2014 – Dossier « Le contrôle biologique des espèces invasives », par Alain Dutartre et Emmanuelle Sarat : http://especes-exotiques-envahissantes.fr/le-controle-biologique-des-especes-invasives/
Plusieurs articles sont venus compléter le dossier de 2014, dont trois portant sur les recherches et les programmes de gestion développés en Afrique du Sud :
- 2016 – Article « La difficile bataille contre les plantes exotiques envahissantes en Afrique du Sud », par Alain Dutartre : http://especes-exotiques-envahissantes.fr/la-difficile-bataille-contre-les-plantes-exotiques-envahissantes-en-afrique-du-sud/
- 2017 – Article « Situation des invasions biologiques et de leur gestion en Afrique du Sud », par Alain Dutartre : http://especes-exotiques-envahissantes.fr/situation-des-invasions-biologiques-et-de-leur-gestion-en-afrique-du-sud-2017/
- 2020 – Article « Invasions biologiques en Afrique du Sud », par Alain Dutartre : http://especes-exotiques-envahissantes.fr/invasions-biologiques-en-afrique-du-sud/
Autres articles sur des essais de contrôle biologique :
- 2020 – Article « Biocontrôle de la Balsamine de l’Himalaya dans les îles britanniques », par Madeleine Freudenreich : http://especes-exotiques-envahissantes.fr/biocontrole-balsamine-himalaya-iles-britanniques/
- 2021 – Article « Premiers essais de contrôle biologique des renouées asiatiques au Royaume-Uni et aux Pays-Bas », par Alain Dutartre : http://especes-exotiques-envahissantes.fr/premiers-essais-de-controle-biologique-des-renouees-asiatiques/
Références citées dans l’article :
Lopez-Núnez F. A., Marchante E., Heleno R., Neto Duarte L., Palhas J., Impson F., Freitas H., Marchante H. (2021). Establishment, spread and early impacts of the first biocontrol agent against an invasive plant in continental Europe. Journal of Environmental Management 290, 112545
- CABI (2019). Acacia longifolia (golden wattle). Datasheet. https://www.cabi.org/isc/datasheet/2312. Version du 20 November 2019.
- Dennill, G. B. (1985). The effect of the gall wasp Trichilogaster acaciaelongifoliae (Hymenoptera: Pteromalidae) on reproductive potential and vegetative growth of the weed Acacia longifolia. Agriculture, ecosystems & environment, 14(1-2), 53-61.
- Dennill, G. B. (1987). Establishment of the gall wasp Trichilogaster acaciaelongifoliae (Pteromalidae) for the biological control of Acacia longifolia in South Africa. Agriculture, ecosystems & environment, 19(2), 155-168.
- Dennill, G. B. (1988). Why a gall former can be a good biocontrol agent: the gall wasp Trichilogaster acaciaelongifoliae and the weed Acacia longifolia. Ecological Entomology, 13(1), 1-9.
- Dennill, G. B., & Gordon, A. J. (1990). Climate-related differences in the efficacy of the Australian gall wasp (Hymenoptera: Pteromalidae) released for the control of Acacia longifolia in South Africa. Environmental entomology, 19(1), 130-136.
- Gibson, M. R., Richardson, D. M., Marchante, E., Marchante, H., Rodger, J. G., Stone, G. N., … & Wilson, J. R. (2011). Reproductive biology of Australian acacias: important mediator of invasiveness?. Diversity and Distributions, 17(5), 911-933.
- Henriksen, M. V., Chapple, D. G., Chown, S. L., & McGeoch, M. A. (2017). Gall wasp biocontrol of invasive Acacia longifolia: implications of strong bottom‐up effects. Ecosphere, 8(12), e02043.
- Kull, C. A., Shackleton, C. M., Cunningham, P. J., Ducatillon, C., Dufour‐Dror, J. M., Esler, K. J., … & Zylstra, M. J. (2011). Adoption, use and perception of Australian acacias around the world. Diversity and Distributions, 17(5), 822-836.
- Marchante, E., Kjøller, A., Struwe, S. & Freitas, H. (2009) Soil recovery after removal of the N2-fixing invasive Acacia longifolia: consequences for ecosystem restoration. Biological Invasions,11, 813–823
- Marchante, H. (2011). Invasion of Portuguese dunes by Acacia longifolia: present status and perspectives for the future (Doctoral dissertation, Universidade de Coimbra (Portugal)).
- Marchante, H., Freitas, H., & Hoffmann, J. H. (2010). Seed ecology of an invasive alien species, Acacia longifolia (Fabaceae), in Portuguese dune ecosystems. American Journal of Botany, 97(11), 1780-1790.
- Marchante, H., Freitas, H., & Hoffmann, J. H. (2011a). Post‐clearing recovery of coastal dunes invaded by Acacia longifolia: is duration of invasion relevant for management success?. Journal of Applied Ecology, 48(5), 1295-1304.
- Marchante, H., Freitas, H., & Hoffmann, J. H. (2011b). Assessing the suitability and safety of a well-known bud-galling wasp, Trichilogaster acaciaelongifoliae, for biological control of Acacia longifolia in Portugal. Biological control, 56(2), 193-201.
- Marchante, H., Marchante, E., Freitas, H., & Hoffmann, J. H. (2015). Temporal changes in the impacts on plant communities of an invasive alien tree, Acacia longifolia. Plant Ecology, 216(11), 1481-1498.
- Morais, M. C., & Freitas, H. (2015). Phenological dynamics of the invasive plant Acacia longifolia in Portugal. Weed Research, 55(6), 555-564.
- Noble, N. S. (1940). Trichilogaster acaciae-longifoliae (Froggatt)(Hymenopt., Chalcidoidea), a wasp causing galling of the flower-buds of Acacia longifolia Willd., A. floribunda Sieber and A. sophorae R. Br. Transactions of the Royal Entomological Society of London, 90, 13-38.
- Pheloung, P. C., Williams, P. A., & Halloy, S. R. (1999). A weed risk assessment model for use as a biosecurity tool evaluating plant introductions. Journal of environmental management, 57(4), 239-251.
- Schwarzländer, M., Hinz, H. L., Winston, R. L., & Day, M. D. (2018). Biological control of weeds: an analysis of introductions, rates of establishment and estimates of success, worldwide. BioControl, 63(3), 319-331.
- Shaw, R. H., Ellison, C. A., Marchante, H., Pratt, C. F., Schaffner, U., Sforza, R. F., & Deltoro, V. (2018). Weed biological control in the European Union: from serendipity to strategy. BioControl, 63(3), 333-347.
- Shaw, R., Schaffner, U., & Marchante, E. (2016). The regulation of biological control of weeds in E urope–an evolving landscape. EPPO Bulletin, 46(2), 254-258.


